细胞培养进口血清进口胎牛血清进口新生牛血清进口猪血清马血清
细胞培养进口血清进口胎牛血清进口新生牛血清进口猪血清马血清 支原体检测盒及标准品常规PCR检测试剂盒荧光定量PCR检测(qPCR法)支原体DNA提取灵敏度标准品(方法验证用)特异性标准品(方法验证用)PCR定量标准品(可用于方法验证)
支原体检测盒及标准品常规PCR检测试剂盒荧光定量PCR检测(qPCR法)支原体DNA提取灵敏度标准品(方法验证用)特异性标准品(方法验证用)PCR定量标准品(可用于方法验证) 支原体祛除试剂细胞中支原体祛除环境支原体祛除水槽支原体祛除
支原体祛除试剂细胞中支原体祛除环境支原体祛除水槽支原体祛除 干细胞培养基
干细胞培养基 DNA/RNA污染祛除DNA/RNA污染祛除试剂DNA污染监测
DNA/RNA污染祛除DNA/RNA污染祛除试剂DNA污染监测 RNA病毒研究试剂RNA病毒检测试剂盒病毒RNA提取
RNA病毒研究试剂RNA病毒检测试剂盒病毒RNA提取 PCR仪器及配套产品DNA污染监测祛除PCR/qPCR仪性能检查PCR试剂PCR试剂盒PCR预混液(冻干粉)热启动聚合酶MB Taq DNA
PCR仪器及配套产品DNA污染监测祛除PCR/qPCR仪性能检查PCR试剂PCR试剂盒PCR预混液(冻干粉)热启动聚合酶MB Taq DNA 微生物PCR检测食品检测类产品食品微生物检测细菌PCR检测
微生物PCR检测食品检测类产品食品微生物检测细菌PCR检测
- 细胞培养进口血清进口胎牛血清进口新生牛血清进口猪血清马血清
- 支原体检测盒及标准品常规PCR检测试剂盒荧光定量PCR检测(qPCR法)支原体DNA提取灵敏度标准品(方法验证用)特异性标准品(方法验证用)PCR定量标准品(可用于方法验证)
- 支原体祛除试剂细胞中支原体祛除环境支原体祛除水槽支原体祛除
- 干细胞培养基
- DNA/RNA污染祛除DNA/RNA污染祛除试剂DNA污染监测
- RNA病毒研究试剂RNA病毒检测试剂盒病毒RNA提取
- PCR仪器及配套产品DNA污染监测祛除PCR/qPCR仪性能检查PCR试剂PCR试剂盒PCR预混液(冻干粉)热启动聚合酶MB Taq DNA
- 微生物PCR检测食品检测类产品食品微生物检测细菌PCR检测
|
|
CAR-T细胞治疗的进展2021-03-19 14:14来源:威正翔禹|缔一生物
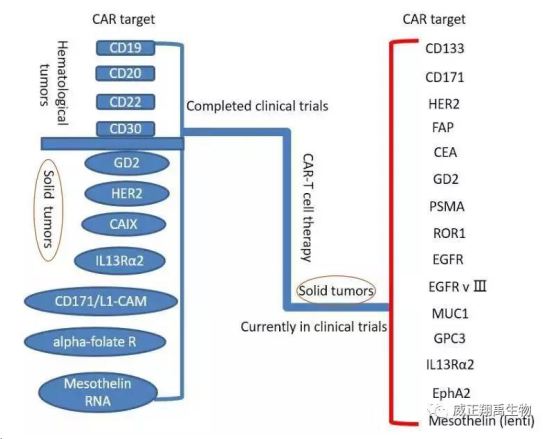
2017年7月15日,我们报道了全球**个CAR-T疗法以全票通过美国FDA评审并上市以来,CAR-T治疗一路高歌猛进,广受瞩目。那么现在,它的进展如何呢? 目前美国已审批上市的CAR-T疗法 截止到2021年2月7日为止,美国FDA审批通过了四种CAR-T治疗产品,具体如下: CAR-T产品Kymriah——治疗【复发性或难治性B细胞急性淋巴细胞白血病】及【复发或难治性大B细胞淋巴瘤】 CAR-T产品Yescarta——治疗【复发性或难治性大B细胞淋巴瘤】 CAR-T产品Tecartus——治疗【复发/难治性套细胞淋巴瘤】 CAR-T产品Liso-cel——治疗【复发性或难治性弥漫大B细胞淋巴瘤】 CAR-T疗法的靶点 上面四种产品均以CD19为靶点。CD19是B细胞系恶性肿瘤的特异性细胞标志物。 其他标志物也用于作为CAR-T的靶点,正处于临床试验阶段。如: BCMA(B细胞成熟抗原)是一种多发性骨髓瘤的标志物。 CD20是一种 B细胞特异性分化抗原,在成熟B细胞和大多数B细胞非霍奇金淋巴瘤表达。 更多CAR-T治疗的靶点可参见下图:
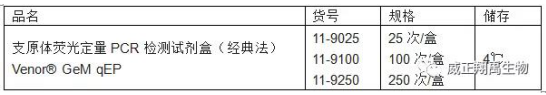
图. 血液肿瘤和实体瘤:已完成和正在进行的CAR-T临床试验(图片来源 Oncotarget) CAR-T对血液肿瘤的治疗大获成功,对许多实体瘤也进行了各种尝试。总体看来,大部分实体瘤的治疗效果远不如血液肿瘤那样显著,只是有些结果令人鼓舞。总体来看,对实体瘤的治疗存在希望,但仍需克服很多问题。 CAR-T疗法需要克服的一些问题 CAR-T疗法的问题包括:治疗实体瘤效果不佳、自体细胞供应不足、治疗后的不良反应、高昂的治疗费用等。 要提高实体瘤的治疗效果,需要设计更好的嵌合抗原受体(CAR)靶向肿瘤细胞,使脱靶效应最小化;增强输注细胞在实体瘤中的定植和聚集;改善实体瘤内输注细胞的增殖和持续存活。目前已取得一些进展。 关于自体细胞供应不足,已有机构使用正常人T细胞来制备CAR-T细胞,只是这种通用CAR-T的T细胞需要用基因编辑的方法进行改造,然后再输到患者体内。不然,通用CAR-T细胞有可能会攻击患者的正常细胞,导致移植物抗宿主病(GvHD)的发生。 CAR-T疗法的副反应主要有细胞因子风暴、脱靶效应以及神经毒性这三方面,也带来了安全问题,也正在得到改善。 总结 截至2021年3月9日,全球注册的CAR-T临床试验已有1234个。而在2020年6月30日,注册的CAR-T试验才只有671个,可见这一领域发展之迅速,也期待有更大的突破。 CAR-T治疗产品的支原体快检 传统支原体检查所需时间较长,不能适应CAR-T细胞治疗产品对支原体快检的需求。 就笔者所知,目前市面上有德国MB(全称Minerva Biolabs)公司提供的【支原体qPCR检测试剂盒(经典法)】和【支原体PCR检测试剂盒(经典法)】,以及配套的【支原体DNA检测试剂盒】和支原体高敏标准品。上述试剂盒已经过厂家的方法验证,符合国际药典的,适合工业和临床以CAR-T为代表的细胞治疗的支原体检查,获得广泛好评。 其信息如下: 1、支原体荧光定量PCR检测试剂盒(经典法) 英文名:Venor? GeM qEP
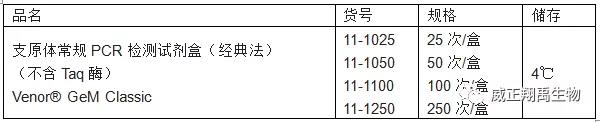
2、支原体常规PCR检测试剂盒(经典法)(不含Taq酶) 英文名:Venor? GeM Classic
3、支原体DNA提取试剂盒 英文名:Venor? GeM Sample Preparation Kit
4、德国MB公司还提供有10CFUTM支原体高敏标准品等一系列方法验证用标准品,用于客户自己对支原体检测试剂盒的方法学验证,尤其是检测限和耐用性的验证。 图片
上一篇: 细胞外基质对细胞增殖的影响
下一篇: 科学家发现卒中后血脑屏障的治疗靶点
|
 细胞培养进口血清
细胞培养进口血清 支原体祛除试剂
支原体祛除试剂 干细胞培养基
干细胞培养基