 细胞培养进口血清进口胎牛血清进口新生牛血清进口猪血清马血清
细胞培养进口血清进口胎牛血清进口新生牛血清进口猪血清马血清 支原体检测盒及标准品常规PCR检测试剂盒荧光定量PCR检测(qPCR法)支原体DNA提取灵敏度标准品(方法验证用)特异性标准品(方法验证用)PCR定量标准品(可用于方法验证)
支原体检测盒及标准品常规PCR检测试剂盒荧光定量PCR检测(qPCR法)支原体DNA提取灵敏度标准品(方法验证用)特异性标准品(方法验证用)PCR定量标准品(可用于方法验证) 支原体祛除试剂细胞中支原体祛除环境支原体祛除水槽支原体祛除
支原体祛除试剂细胞中支原体祛除环境支原体祛除水槽支原体祛除 干细胞培养基
干细胞培养基 DNA/RNA污染祛除DNA/RNA污染祛除试剂DNA污染监测
DNA/RNA污染祛除DNA/RNA污染祛除试剂DNA污染监测 RNA病毒研究试剂RNA病毒检测试剂盒病毒RNA提取
RNA病毒研究试剂RNA病毒检测试剂盒病毒RNA提取 PCR仪器及配套产品DNA污染监测祛除PCR/qPCR仪性能检查PCR试剂PCR试剂盒PCR预混液(冻干粉)热启动聚合酶MB Taq DNA
PCR仪器及配套产品DNA污染监测祛除PCR/qPCR仪性能检查PCR试剂PCR试剂盒PCR预混液(冻干粉)热启动聚合酶MB Taq DNA 微生物PCR检测食品检测类产品食品微生物检测细菌PCR检测
微生物PCR检测食品检测类产品食品微生物检测细菌PCR检测
- 细胞培养进口血清进口胎牛血清进口新生牛血清进口猪血清马血清
- 支原体检测盒及标准品常规PCR检测试剂盒荧光定量PCR检测(qPCR法)支原体DNA提取灵敏度标准品(方法验证用)特异性标准品(方法验证用)PCR定量标准品(可用于方法验证)
- 支原体祛除试剂细胞中支原体祛除环境支原体祛除水槽支原体祛除
- 干细胞培养基
- DNA/RNA污染祛除DNA/RNA污染祛除试剂DNA污染监测
- RNA病毒研究试剂RNA病毒检测试剂盒病毒RNA提取
- PCR仪器及配套产品DNA污染监测祛除PCR/qPCR仪性能检查PCR试剂PCR试剂盒PCR预混液(冻干粉)热启动聚合酶MB Taq DNA
- 微生物PCR检测食品检测类产品食品微生物检测细菌PCR检测
|
|
蛋白质组学再立战功:揭示了BCAT1在癌细胞转移中的重要作用2021-12-03 14:38来源:威正翔禹|缔一生物
癌症是对人类健康威胁**的疾病之一。根据世界卫生组织(WHO)的统计,2018 年全球新发癌症病例达到 1,807 万例,其中肺癌 209 万例,发病率名列前茅。
中国癌症新发患者人数也在逐年增加,根据国家癌症中心发布的全国最新癌症数据,2015 年全国新发恶性肿瘤病例数约 392.9 万例,肺癌位居发病首位。
 肺癌患病率逐年攀升,转移是肺癌高死亡率的主要原因之一,严重危害人类公共健康。 肺癌是如何转移的? 哪些因素会影响肺癌转移? 如何断了癌细胞后路,避免其转移? 这些问题一直困扰着研究人员。 近日,《Theranostics》上发表了一篇标题为:“Proteomic analysis of lung cancer cells reveals a critical role of BCAT1 in cancer cell metastasis”的论文,或许可以在一定程度上回答上述问题。  图片来源:https://www.thno.org/v11p9705.htm 点击文末阅读原文,即可获得完整文献 浓缩精华版: 研究人员发现:在转移性肺癌细胞和肺癌患者的转移性组织中,分支链氨基酸代谢的关键酶BCAT1蛋白水平呈现过表达状态。通过数据分析分析得出结论:BCAT1转录的增加,与肺癌患者总生存率较低之间存在关联性。 感兴趣的小伙伴可以接着往下看,有详细版。  在过去的十年中,基因组测序越来越多地被应用到转移性肿瘤突变谱的研究中 [1,2]。已有一些研究,对肺癌患者标本进行了全面的蛋白质基因组学研究,绘制了呈现了原发肿瘤相对于肿瘤旁“正常”组织的蛋白质组图 [3,4]。然而,关于转移性肺癌的蛋白质组水平的相关研究仍然不足。 我们已经知道,氨基酸代谢在肿瘤发生和转移中起重要作用。 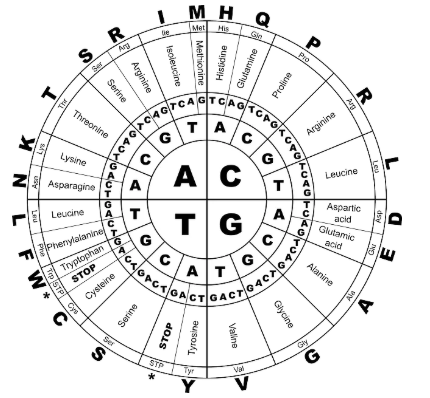 氨基酸密码子对照表 支链氨基酸(BCAA)到α-酮戊二酸(α-KG)的转氨基反应,由胞质BCAT1和线粒体BCAT2两种类型的bcat基因催化。该反应产生谷氨酸,而谷氨酸又可以被肿瘤细胞优先利用以促进生存[5]。 点击下方小程序 了解细胞培养相关血清产品详情
由此得到的支链酮酸(BCKA)进一步分解为乙酰辅酶A和琥珀酰辅酶A,它们是TCA循环的中间体[6]。BCAT1的过表达与髓样白血病[7]、胶质瘤[8]和非小细胞肺癌[9]的癌症进展有关,而增加BCAA摄取对于维持NSCLC[10]的肿瘤发生很重要。然而,BCAT1的表达过程,是否在转移性肿瘤中出现紊乱?在潜在的迁移过程中发挥作用?这些目前尚不清楚。 为了确定与肺癌转移状态相关的蛋白质组学的变化,研究人员用到了一种同位素标记(SILAC:细胞培养稳定同位素标记,在细胞培养过条件下,用含有轻、重同位素标记氨基酸的培养基,进行细胞培养,若干代后,细胞中的蛋白质被稳定标记上同位素)的定量质谱分析。 利用原发性肺腺癌A549细胞系(指定L0)和L0细胞进行了三轮BALB/c Nude小鼠体内选择,产生脊柱转移细胞(指定L2和L6)[11]。然后,分别在“轻、中、重”三种同位素标记的培养基进行培养,稳定标记后进行质谱定量分析。 得到结果1
随后,作者又比较分析了四对,来自肿瘤患者样本的原发和转移性肿瘤组织进行蛋白质组学。 采用串联质谱(TMT)标记和质谱定量分析方法检测蛋白表达,利用TCGA数据进行分析。 得到结果2
接着,研究人员利用A549细胞系,进行了一系列细胞学实验以及分子实验:Western blot、trans-well、RNA干扰等,以及小鼠体内实验,进一步探究BCAT1在转移中的作用。 说到细胞培养,自然离不开动物血清,Ausbian进口特级胎牛血清,内毒素低(≤3EU/ml),品质稳定,点击下方小程序了解更多产品详情。
得到结果3
为了深入了解BCAT1介导的转移的机制,研究人员检测了与干细胞和上皮-间质转化(EMT)相关基因的表达。 得到结果4
SOX2是维持胚胎干细胞和肿瘤干细胞可塑性的转录因子,它的过表达促进了肺癌的转移。在已有研究中,SOX2的表达增加可能会使L0细胞进入低分化状态,迁移能力增加。 文章作者从先前的研究[11]中重新分析了这些A549细胞的RNA-seq数据。 得到结果5
然而,在先前的SILAC实验结果中,转移细胞中包括CTNNB1和DVL2在内的Wnt信号蛋白减少。He等人之前的一项研究也表明,过表达SOX2可能通过上调A549细胞[12]中的GSK3β,导致Wnt/β-catenin信号通路的抑制。 因此,作者假设SOX2通过β-catenin抑制Wnt信号,维持转移细胞的未分化状态。 为了验证这一假设,研究人员用几种不同的方式:荧光成像、流式细胞术、Western blot、Real-time PCR,确定了BCAT1在转移性A549细胞中促进了SOX2的表达,这一新的途径可能是肺癌细胞干性的重要调控因子。 得到结果6
TET2调控的许多基因中有编码micro-RNAs的基因,已有研究表明miR200家族成员是SOX2的负调控因子。 这提出了一种可能性: 即bcat介导的α-KG的减少导致miR200家族成员的高甲基化,并解除了SOX2的翻译抑制。 分析显示miR200c的表达与BCAT1呈负相关。 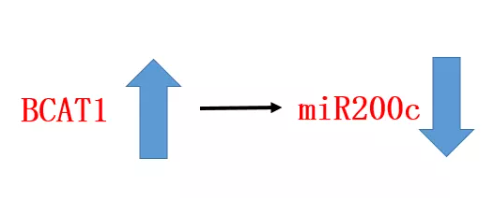 有报道称:miR-200c表达的丢失在NSCLC中诱导了侵袭性表型。研究人员测量了miR200c,以及其他后续实验。 得到结果7
因此,研究人员认为: BCAT1-α-KG-miR200c-SOX2 调控途径成立! 综上所述,研究发现BCAT1在转移性肺癌细胞中表达上调,调控其迁移转移,并与不良预后相关。该研究确定了一条新的通路,其中α-KG是转移性肺癌细胞中BCAT1和SOX2表达转录后调控之间的关键代谢信号传导中间体。 这些发现可能为靶向肺癌转移过程的治疗开辟新的策略。 如果你对本公司产品感兴趣,想要了解更多,欢迎访问 北京缔一生物官网:www.dyshengwu.com 或联系北京缔一生物公司 咨询热线: 400-166-8600 010-84118494 021-64186645 13811167915 咨询QQ: 1580434811 咨询QQ: 1258888686 客服邮箱:servicebj@viansaga.com 客服邮箱:servicesh@viansaga.com 声明:本网站所有注明“来源:缔一生物”的内容,版权均属于北京缔一生物网站所有,受到知识产权的法律保护。如需引用、转载,须注明来源及原文链接。如内容涉及实质性修改,须来电获取书面授权,且转载时,须注明“来源:缔一生物”。 最终解释权归缔一生物所有。 上一篇: 快来查收你的**份新年礼物!
下一篇: 关于HIV的****知识,这期必看!
|
 细胞培养进口血清
细胞培养进口血清 支原体祛除试剂
支原体祛除试剂 干细胞培养基
干细胞培养基



